Peptidit ovat luokka yhdisteitä, jotka muodostuvat yhdistämällä useita aminohappoja peptidisidosten kautta.Ne ovat kaikkialla elävissä organismeissa.Tähän mennessä elävistä organismeista on löydetty kymmeniä tuhansia peptidejä.Peptideillä on tärkeä rooli eri järjestelmien, elinten, kudosten ja solujen toiminnallisten toimintojen säätelyssä ja elämäntoiminnassa, ja niitä käytetään usein funktionaalisessa analyysissä, vasta-ainetutkimuksessa, lääkekehityksessä ja muilla aloilla.Biotekniikan ja peptidisynteesitekniikan kehittyessä yhä enemmän peptidilääkkeitä on kehitetty ja käytetty klinikoilla.
Peptidimodifikaatioita on laaja valikoima, jotka voidaan yksinkertaisesti jakaa modifikaation jälkeisiin ja prosessimuunnoksiin (käyttämällä johdettua aminohappomodifikaatiota) ja N-terminaaliseen modifikaatioon, C-terminaaliseen modifikaatioon, sivuketjun modifikaatioon, aminohappomodifikaatioon, luuston modifikaatioon, jne. muokkauspaikasta riippuen (kuva 1).Tärkeänä keinona muuttaa peptidiketjujen pääketjun rakennetta tai sivuketjuryhmiä peptidimodifikaatiolla voidaan tehokkaasti muuttaa peptidiyhdisteiden fysikaalisia ja kemiallisia ominaisuuksia, lisätä vesiliukoisuutta, pidentää vaikutusaikaa in vivo, muuttaa niiden biologista jakautumista, eliminoida immunogeenisyyden. , vähentää myrkyllisiä sivuvaikutuksia jne. Tässä artikkelissa esitellään useita merkittäviä peptidimuunnosstrategioita ja niiden ominaisuuksia.
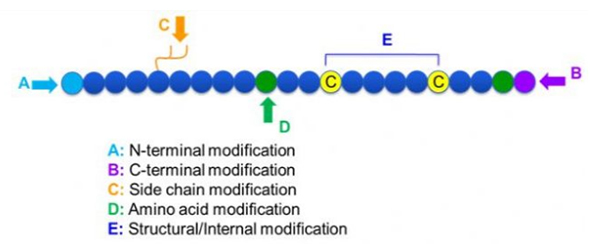
1. Pyöräily
Syklisillä peptideillä on monia sovelluksia biolääketieteessä, ja monet luonnolliset peptidit, joilla on biologista aktiivisuutta, ovat syklisiä peptidejä.Koska sykliset peptidit ovat yleensä jäykempiä kuin lineaariset peptidit, ne ovat erittäin vastustuskykyisiä ruoansulatusjärjestelmälle, voivat selviytyä ruoansulatuskanavassa ja niillä on vahvempi affiniteetti kohdereseptoreihin.Syklisointi on suorin tapa syntetisoida syklisiä peptidejä, erityisesti peptideille, joilla on suuri rakenteellinen luuranko.Syklisointitilan mukaan se voidaan jakaa sivuketjun sivuketjun tyyppiin, pääte - sivuketjutyyppiin, pääte - päätetyyppiin (päästä päähän -tyyppi).
(1) sivuketjusta sivuketjuun
Yleisin sivuketjun sivuketjun syklisointityyppi on disulfidisilta kysteiinitähteiden välillä.Tämä syklisointi saadaan aikaan siten, että kysteiinitähteiden parista poistetaan suojaus ja hapetetaan sitten disulfidisidoksia.Polysyklinen synteesi voidaan saavuttaa poistamalla selektiivisesti sulfhydryylisuojaryhmät.Syklisointi voidaan tehdä joko dissosiaatiota jälkeisessä liuottimessa tai esidissosiaatiohartsissa.Hartseilla tapahtuva syklisointi voi olla vähemmän tehokasta kuin liuotinsyklisointi, koska hartseilla olevat peptidit eivät helposti muodosta syklisoituja konformaatioita.Toinen sivuketju-sivuketjusyklisoinnin tyyppi on amidirakenteen muodostuminen asparagiinihappo- tai glutamiinihappotähteen ja emäsaminohapon välille, mikä edellyttää, että sivuketjun suojaryhmä on voitava poistaa selektiivisesti polypeptidistä joko hartsilla tai dissosioinnin jälkeen.Kolmas sivuketju-sivuketjusyklisoinnin tyyppi on difenyylieettereiden muodostaminen tyrosiinilla tai p-hydroksifenyyliglysiinillä.Tämän tyyppistä syklisointia luonnontuotteissa esiintyy vain mikrobituotteista, ja syklisointituotteilla on usein potentiaalista lääkearvoa.Näiden yhdisteiden valmistus vaatii ainutlaatuisia reaktio-olosuhteita, joten niitä ei usein käytetä tavanomaisten peptidien synteesissä.
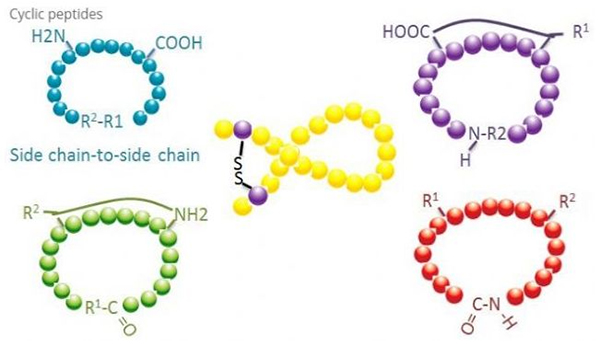
(2) terminaalista sivuketjuun
Terminaalisen puolen ketjun syklisointi käsittää tavallisesti C-terminaalin lysiinin tai ornitiinin sivuketjun aminoryhmän kanssa tai N-pään asparagiinihapon tai glutamiinihapon sivuketjun kanssa.Muu polypeptidisyklisointi tehdään muodostamalla eetterisidoksia terminaalisen C ja seriini- tai treoniinisivuketjujen välille.
(3) Terminaali tai head-to-tail-tyyppi
Ketjupolypeptidit voidaan joko syklisoida liuottimessa tai kiinnittää hartsiin sivuketjun syklisoinnilla.Alhaisia peptidipitoisuuksia tulisi käyttää liuottimen keskittämisessä peptidien oligomeroitumisen välttämiseksi.Päästä häntään synteettisen rengaspolypeptidin saanto riippuu ketjupolypeptidin sekvenssistä.Siksi ennen syklisten peptidien valmistamista suuressa mittakaavassa tulisi ensin luoda kirjasto mahdollisista ketjutetuista johtopeptideistä, mitä seuraa syklisointi, jotta löydetään sekvenssi, jolla on parhaat tulokset.
2. N-metylointi
N-metylaatiota esiintyy alun perin luonnollisissa peptideissä ja se sisällytetään peptidisynteesiin vetysidosten muodostumisen estämiseksi, mikä tekee peptideistä vastustuskykyisempiä biohajoamista ja puhdistumaa vastaan.Peptidien synteesi käyttämällä N-metyloituja aminohappojohdannaisia on tärkein menetelmä.Lisäksi voidaan käyttää myös N-(2-nitrobentseenisulfonyylikloridi)polypeptidi-hartsivälituotteiden Mitsunobu-reaktiota metanolin kanssa.Tätä menetelmää on käytetty N-metyloituja aminohappoja sisältävien syklisten peptidikirjastojen valmistukseen.
3. Fosforylaatio
Fosforylaatio on yksi yleisimmistä translaation jälkeisistä modifikaatioista luonnossa.Ihmissoluissa yli 30 % proteiineista on fosforyloitunut.Fosforylaatiolla, erityisesti reversiibelillä fosforylaatiolla, on tärkeä rooli monien soluprosessien, kuten signaalitransduktion, geeniekspression, solusyklin ja sytoskeleton säätelyn ja apoptoosin säätelyssä.
Fosforylaatiota voidaan havaita useissa aminohappotähteissä, mutta yleisimmät fosforylaatiokohteet ovat seriini-, treoniini- ja tyrosiinitähteet.Fosfotyrosiini, fosfotreoniini ja fosfoseriinijohdannaiset voidaan joko viedä peptideihin synteesin aikana tai muodostaa peptidisynteesin jälkeen.Selektiivinen fosforylaatio voidaan saada aikaan käyttämällä seriinin, treoniinin ja tyrosiinin tähteitä, jotka selektiivisesti poistavat suojaryhmiä.Jotkut fosforylaatioreagenssit voivat myös lisätä fosforihapporyhmiä polypeptidiin jälkimodifioinnin avulla.Viime vuosina lysiinin paikkaspesifistä fosforylaatiota on saavutettu käyttämällä kemiallisesti selektiivistä Staudinger-fosfiittireaktiota (kuva 3).
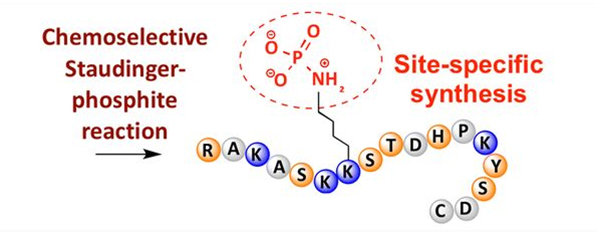
4. Myristoylaatio ja palmitoylaatio
N-pään asylointi rasvahapoilla mahdollistaa peptidien tai proteiinien sitoutumisen solukalvoihin.N-pään myridamoyloitu sekvenssi mahdollistaa Src-perheen proteiinikinaasien ja käänteistranskriptaasi-Gaq-proteiinien kohdistamisen sitoutumaan solukalvoihin.Myristiinihappo liitettiin hartsi-polypeptidin N-päähän käyttämällä tavanomaisia kytkentäreaktioita, ja tuloksena saatu lipopeptidi voitiin dissosioida standardiolosuhteissa ja puhdistaa RP-HPLC:llä.
5. Glykosylaatio
Glykopeptidit, kuten vankomysiini ja teikolaniini, ovat tärkeitä antibiootteja lääkeresistenttien bakteeri-infektioiden hoidossa, ja muita glykopeptidejä käytetään usein immuunijärjestelmän stimuloimiseen.Lisäksi, koska monet mikrobiantigeenit ovat glykosyloituneita, on erittäin tärkeää tutkia glykopeptidejä infektion terapeuttisen vaikutuksen parantamiseksi.Toisaalta on havaittu, että kasvainsolujen solukalvon proteiineissa on epänormaalia glykosylaatiota, minkä vuoksi glykopeptideillä on tärkeä rooli syövän ja kasvainten immuunipuolustuksen tutkimuksessa.Glykopeptidit valmistetaan Fmoc/t-Bu-menetelmällä.Glykosyloituja tähteitä, kuten treoniinia ja seriiniä, viedään usein polypeptideihin pentafluorifenoliesteriaktivoiduilla fMOC:illa glykosyloitujen aminohappojen suojaamiseksi.
6. Isopreeni
Isopentadienylaatio tapahtuu kysteiinitähteissä sivuketjussa lähellä C-terminaalia.Proteiini-isopreeni voi parantaa solukalvoaffiniteettia ja muodostaa proteiini-proteiinivuorovaikutusta.Isopentadienoituja proteiineja ovat tyrosiinifosfataasi, pieni GTaasi, kokaperonimolekyylit, tuman laminaatti ja sentromeeriset sitoutumisproteiinit.Isopreenipolypeptidejä voidaan valmistaa käyttämällä isopreenia hartseilla tai lisäämällä kysteiinijohdannaisia.
7. Polyetyleeniglykolin (PEG) muunnos
PEG-modifikaatiota voidaan käyttää parantamaan proteiinin hydrolyyttistä stabiilisuutta, biologista jakautumista ja peptidin liukoisuutta.PEG-ketjujen lisääminen peptideihin voi parantaa niiden farmakologisia ominaisuuksia ja myös estää peptidien hydrolyysiä proteolyyttisten entsyymien vaikutuksesta.PEG-peptidit läpäisevät glomerulaarisen kapillaarin poikkileikkauksen helpommin kuin tavalliset peptidit, mikä vähentää huomattavasti munuaispuhdistumaa.PEG-peptidien pidennetyn aktiivisen puoliintumisajan in vivo ansiosta normaali hoitotaso voidaan ylläpitää pienemmillä annoksilla ja harvemmin käytetyillä peptidilääkkeillä.PEG-muuntamisella on kuitenkin myös negatiivisia vaikutuksia.Suuret määrät PEG:tä estävät entsyymiä hajottamasta peptidiä ja vähentävät myös peptidin sitoutumista kohdereseptoriin.Mutta PEG-peptidien alhaista affiniteettia kompensoi yleensä niiden pidempi farmakokineettinen puoliintumisaika, ja koska PEG-peptidit ovat kehossa pidempään, ne imeytyvät todennäköisemmin kohdekudoksiin.Siksi PEG-polymeerimääritykset tulisi optimoida optimaalisten tulosten saavuttamiseksi.Toisaalta PEG-peptidit kerääntyvät maksaan vähentyneen munuaispuhdistuman vuoksi, mikä johtaa makromolekyyliseen oireyhtymään.Siksi PEG-modifikaatiot on suunniteltava huolellisemmin, kun peptidejä käytetään lääketestaukseen.
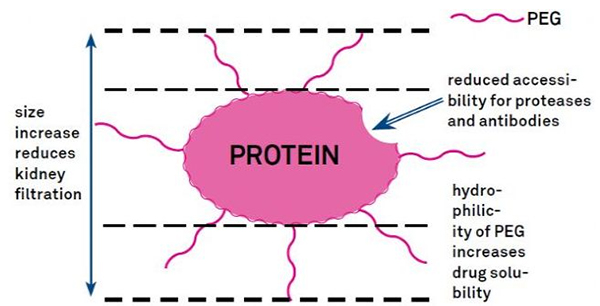
PEG-muuntajien yleiset modifikaatioryhmät voidaan karkeasti tiivistää seuraavasti: Amino (-amiini) -NH2, aminometyyli-Ch2-NH2, hydroksi-OH, karboksi-Cooh, sulfhydryyli (-tioli) -SH, Maleimidi -MAL, sukkinimidikarbonaatti - SC, sukkinimidiasetaatti -SCM, sukkinimidipropionaatti -SPA, n-hydroksisukkinimidi -NHS, akrylaatti-ch2ch2cooh, aldehydi -CHO (kuten propionald, butyrALD), akryyliemäs (-akrylaatti-acrl), bioatsido-atsidi Biotiini, fluoreseiini, glutaryyli-GA, akrylaattihydratsidi, alkyyni-alkyeni, p-tolueenisulfonaatti-OT:t, sukkinimidisukkinaatti-SS jne. PEG-johdannaiset karboksyylihappojen kanssa voidaan kytkeä n-pään amiineihin tai lysiinin sivuketjuihin.Aminoaktivoitu PEG voidaan kytkeä asparagiinihappo- tai glutamiinihapposivuketjuihin.Mal-aktivoitu PEG voidaan konjugoida merkaptaaniin, jonka kysteiinisivuketjut ovat täysin suojattuna [11].PEG-muuntajat luokitellaan yleensä seuraavasti (huomaa: mPEG on metoksi-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) suoraketjuinen PEG-muuntaja
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) bifunktionaalinen PEG-muuntaja
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) haarautuva PEG-muuntaja
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinointi
Biotiini voi sitoutua vahvasti avidiiniin tai streptavidiiniin, ja sitoutumisvoimakkuus on jopa lähellä kovalenttista sidosta.Biotiinileimattuja peptidejä käytetään yleisesti immunomäärityksessä, histosytokemiassa ja fluoresenssipohjaisessa virtaussytometriassa.Leimattuja antibiotiinivasta-aineita voidaan käyttää myös biotinyloitujen peptidien sitomiseen.Biotiinileimat kiinnitetään usein lysiinin sivuketjuun tai N-päähän.6-aminokapronihappoa käytetään usein sidoksena peptidien ja biotiinin välillä.Sidos sitoutuu joustavasti alustaan ja sitoutuu paremmin steeristen esteiden läsnä ollessa.
9. Fluoresoiva merkintä
Fluoresoivaa leimaamista voidaan käyttää polypeptidien jäljittämiseen elävissä soluissa sekä entsyymien ja vaikutusmekanismien tutkimiseen.Tryptofaani (Trp) on fluoresoiva, joten sitä voidaan käyttää luontaiseen leimaamiseen.Tryptofaanin emissiospektri riippuu perifeerisestä ympäristöstä ja pienenee liuottimen polaarisuuden pienentyessä, mikä on ominaisuus, joka on hyödyllinen peptidirakenteen ja reseptorisitoutumisen havaitsemisessa.Tryptofaanifluoresenssi voidaan sammuttaa protonoidulla asparagiinihapolla ja glutamiinihapolla, mikä saattaa rajoittaa sen käyttöä.Dansyylikloridiryhmä (Dansyl) on erittäin fluoresoiva, kun se on sitoutunut aminoryhmään, ja sitä käytetään usein aminohappojen tai proteiinien fluoresoivana leimana.
Fluoresenssiresonanssi Energiamuunnos (FRET) on hyödyllinen entsyymitutkimuksissa.Kun FRET:iä käytetään, substraattipolypeptidi sisältää tavallisesti fluoresenssin leimaavan ryhmän ja fluoresenssin sammuttavan ryhmän.Leimatut fluoresoivat ryhmät sammutetaan sammuttimella ei-fotoni-energiansiirrolla.Kun peptidi irtoaa kyseisestä entsyymistä, leimausryhmä emittoi fluoresenssia.
10. Häkkipolypeptidit
Häkkipeptideissä on optisesti poistettavia suojaryhmiä, jotka suojaavat peptidiä sitoutumiselta reseptoriin.Kun peptidi altistetaan UV-säteilylle, se aktivoituu ja palauttaa affiniteetin reseptoriin.Koska tätä optista aktivaatiota voidaan ohjata ajan, amplitudin tai sijainnin mukaan, häkkipeptidejä voidaan käyttää soluissa tapahtuvien reaktioiden tutkimiseen.Häkkipolypeptidien yleisimmin käytetyt suojaryhmät ovat 2-nitrobentsyyliryhmät ja niiden johdannaiset, jotka voidaan liittää peptidisynteesiin suojaavien aminohappojohdannaisten kautta.Aminohappojohdannaisia, joita on kehitetty, ovat lysiini, kysteiini, seriini ja tyrosiini.Aspartaatti- ja glutamaattijohdannaisia ei kuitenkaan käytetä yleisesti, koska ne ovat alttiita syklisoitumiselle peptidisynteesin ja dissosiaation aikana.
11. Polyantigeeninen peptidi (MAP)
Lyhyet peptidit eivät yleensä ole immuuneja, ja ne on kytkettävä kantajaproteiineihin vasta-aineiden tuottamiseksi.Polyantigeeninen peptidi (MAP) koostuu useista identtisistä peptideistä, jotka on liitetty lysiiniytimiin, jotka voivat spesifisesti ekspressoida voimakkaita immunogeenejä ja joita voidaan käyttää peptidi-kantajaproteiini-parien valmistukseen.MAP-polypeptidit voidaan syntetisoida kiinteäfaasisynteesillä MAP-hartsilla.Epätäydellinen kytkentä johtaa kuitenkin puuttuviin tai typistettyihin peptidiketjuihin joissakin haaroissa, eikä se siten osoita alkuperäisen MAP-polypeptidin ominaisuuksia.Vaihtoehtona peptidit voidaan valmistaa ja puhdistaa erikseen ja sitten kytkeä MAP:iin.Peptidiytimeen kiinnitetty peptidisekvenssi on hyvin määritelty ja helposti karakterisoitava massaspektrometrialla.
Johtopäätös
Peptidimodifiointi on tärkeä keino peptidien suunnittelussa.Kemiallisesti modifioidut peptidit eivät voi vain ylläpitää korkeaa biologista aktiivisuutta, vaan myös tehokkaasti välttää immunogeenisyyden ja toksisuuden haitat.Samaan aikaan kemiallinen modifiointi voi antaa peptideille uusia erinomaisia ominaisuuksia.Viime vuosina CH-aktivointimenetelmää polypeptidien jälkimodifiointiin on kehitetty nopeasti, ja monia tärkeitä tuloksia on saavutettu.
Postitusaika: 20.3.2023
